Ny forskning i Nature fra CARD: effektiv kræftmedicin virker modsat end hidtil troet
Forskere fra DG-centeret Center for Autofagi, Recirkulering og Sygdom (CARD) ved Kræftens Bekæmpelses Center for Kræftforskning står bag ny forklaring på kræftmedicins virkning samt på grundlæggende processer under celledeling.

Professor og enhedsleder Jiri Bartek og seniorforsker Apolinar Maya-Mendoza fra DG-centeret CARD hos Kræftens Bekæmpelses Center for Kræftforskning står sammen bag ny forskning, der viser, at kræftmedicin mod arveligt bryst- og æggestokkræft virker modsat, end hvad man hidtil har troet. En viden, der potentielt kan føre til bedre behandlinger af kræftsygdomme. Studiet er netop publiceret i det videnskabelige tidsskrift Nature Letters.
Kroppens celler udsættes konstant for skader og slid og erstattes efterhånden af nye celler ved hjælp af celledeling, hvor en celle deler sig i to. Samme princip gælder for kræftceller, der ofte kan dele sig hurtigere og hyppigere end normale celler. Når kroppen gennemgår kræftbehandling, går en del af behandlingen derfor ud på at bremse kræftcellernes delingsproces for derigennem at standse væksten af kræft.
Kræftmedicin som Olaparib og Veliparib er eksempler på lægemidler, der netop har den virkning. De bliver brugt i behandlingen af blandt andet arvelig bryst- og æggestokkræft, der skyldes fejl i såkaldte BRCA-gener. Lægemidler som disse kaldes PARP-hæmmere, og som navnet antyder, virker medicinen ved at hæmme proteinet PARP, der indgår i den cellulære reparationsproces.
Indtil nu har forskere verden over troet, at virkningen bag disse PARP-hæmmere skyldes, at de forhindrer kræftceller med for lidt BRCA i at reparere DNA-skader og derved blokerer for DNA-kopieringen. Men forskningen fra CARD viser, at der er tale om den stik modsatte effekt. Seniorforsker Apolinar Maya-Mendoza, forklarer:
”PARP-hæmmere virker ved at øge hastigheden på DNA-kopieringen i kræftcellerne. Samtidig bliver fejl i DNA’et, som opstår under kopieringen – såkaldt replikationsstress – som ellers virker som tegn til cellen om at standse sin deling, overset. Hos kræftceller, der mangler BRCA-genet, fører det til, at der ophobes så mange fejl i cellernes gener, at de til sidst dør.” (Se illustration):
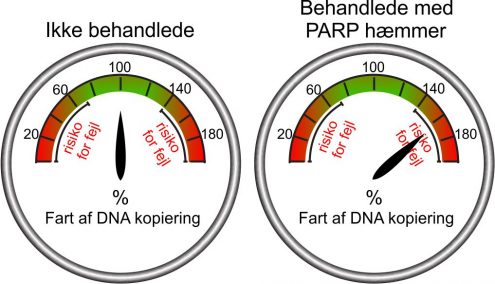
Proteiner styrer hastigheden af cellers DNA-kopiering
Den nye forskning viser desuden, hvilken rolle PARP-proteinet har, når det ikke er hæmmet. Forskerne fandt ud af, at PARP indgår i et netværk af proteiner, som tilsammen styrer, hvor hurtigt DNA-kopieringen sker. Hastigheden er helt afgørende for kopieringsprocessen, da det hverken må gå for hurtigt eller for langsomt. Forskernes nye resultater viser, at DNA-kopieringen skal ske med en hastighed, der ligger indenfor et helt bestemt interval, for at undgå øget risiko for, at der opstår fejl i DNA’et, som enten kan føre til udviklingen af kræft eller til, at cellerne dør.
Forskningsresultatet fra CARD bringer dermed ny viden omkring celledeling, hvilket er en af de mest fundamentale kropslige egenskaber.
”Vores nye resultater er overraskende for den videnskabelige verden, og åbner for nye måder at se på DNA kopiering og udvikling af kræft som sygdom – og ikke kun for kræft, der skyldes fejl i BRCA,” siger Jiri Bartek og suppleres af Maya-Mendoza:
”Ved at forstå præcist, hvilken effekt forskellige behandlinger har i kræftcellerne, bliver vi bedre i stand til at regne ud, hvilke behandlinger – eventuelt i kombination – der virker bedst. Det kan føre til nye og bedre behandlinger i fremtiden.”
Find den videnskabelige artikel hos Nature her
Yderligere information om forskningen kan findes hos Kræftens Bekæmpelse her
